XPOVIO® Menerima Persetujuan Penggantian Biaya di Korea Selatan untuk Indikasi Multiple Myeloma Kedua
– XPOVIO® adalah inhibitor XPO1 pertama yang disetujui untuk penggantian biaya oleh Layanan Asuransi Kesehatan Nasional Korea Selatan (NHIS) untuk pengobatan pasien dewasa dengan multiple myeloma (MM).
– Di Korea Selatan, XPOVIO® telah disetujui untuk tiga indikasi pada MM dan limfoma sel B besar difus (DLBCL), dan dua dari indikasi yang disetujui ini telah dimasukkan dalam skema penggantian biaya nasional.
SHANGHAI dan HONG KONG, 1 Maret 2026 /PRNewswire/ — Antengene Corporation Limited ("Antengene", SEHK: 6996.HK), perusahaan bioteknologi global terkemuka yang inovatif dan berada di tahap komersial yang berdedikasi untuk menemukan, mengembangkan, dan mengkomersialkan obat-obatan first-in-class dan/atau best-in-class untuk penyakit autoimun, tumor padat, dan indikasi keganasan hematologi, mengumumkan bahwa Layanan Asuransi Kesehatan Nasional Korea Selatan (NHIS) telah menyetujui penggantian biaya XPOVIO® (selinexor) dalam kombinasi dengan bortezomib dan dexamethasone untuk pengobatan pasien dewasa dengan multiple myeloma (MM) setelah satu terapi sebelumnya. Penggantian biaya ini telah berlaku pada 1 Maret 2026. Ini menandai indikasi XPOVIO® kedua yang disetujui untuk penggantian biaya di Korea Selatan.
Sementara Antengene terus memperluas jejaknya di seluruh wilayah Asia Pasifik, Perusahaan tetap berkomitmen untuk meningkatkan akses pasien terhadap terapi inovatifnya. Hingga saat ini, XPOVIO® telah disetujui di Korea Selatan untuk tiga indikasi pada MM dan limfoma sel B besar difus (DLBCL), keduanya merupakan keganasan hematologi utama. Dua dari indikasi ini telah disetujui untuk penggantian biaya, termasuk XPOVIO® dalam kombinasi dengan dexamethasone untuk pengobatan pasien dewasa dengan MM kambuh atau refraktori (R/R MM) yang telah menerima setidaknya empat terapi sebelumnya, serta indikasi yang baru diganti biayanya. Dengan cakupan penggantian biaya yang diperluas, XPOVIO® diharapkan dapat memberikan manfaat bagi populasi pasien yang lebih luas dan lebih berkontribusi pada pengelolaan keganasan hematologi di Korea Selatan.
Dengan mekanisme kerja yang baru, XPOVIO® adalah inhibitor XPO1 selektif oral pertama di dunia yang disetujui. XPOVIO® telah disetujui di sepuluh negara dan wilayah di APAC, dan telah dimasukkan dalam skema asuransi nasional di lima pasar tersebut (daratan Tiongkok, pasar Taiwan, Australia, Singapura, dan Korea Selatan). Ke depan, Antengene akan terus mengupayakan akses yang lebih luas untuk XPOVIO® di seluruh pasar APAC.
Tentang Antengene
Antengene Corporation Limited ("Antengene", SEHK: 6996.HK) adalah perusahaan bioteknologi global yang didorong oleh R&D dan berada di tahap komersial yang berfokus pada pengembangan terapi first-in-class/best-in-class untuk penyakit dengan kebutuhan medis yang belum terpenuhi secara signifikan. Pipelinenya mencakup dari tahap praklinis hingga komersial dan mencakup beberapa program yang ditemukan secara internal, termasuk ATG-022 (CLDN18.2 ADC), ATG-037 (inhibitor CD73 oral), ATG-101 (antibodi bispesifik PD-L1 × 4-1BB), dan ATG-042 (inhibitor PRMT5-MTA oral).
Antengene juga telah mengembangkan AnTenGager , platform T cell engager 2.0 milik sendiri yang menampilkan pengikatan bivalen "2+1" untuk target yang mengekspresikan rendah, penyamaran hambatan sterik, dan urutan CD3 milik sendiri dengan kinetika on/off cepat untuk meminimalkan sindrom pelepasan sitokin (CRS) dan meningkatkan kemanjuran. Karakteristik ini mendukung penerapan platform yang luas di seluruh penyakit autoimun, tumor padat, dan keganasan hematologi, dengan program yang menargetkan CD19 x CD3 (ATG-201 untuk penyakit autoimun terkait sel B), CDH6 x CD3 (ATG-106 untuk kanker ovarium dan kanker ginjal), ALPPL2 x CD3 (ATG-112 untuk tumor ginekologi dan kanker paru-paru sel bukan kecil), LY6G6D x CD3 (ATG-110 untuk kanker kolorektal stabil mikrosatelit), GPRC5D x CD3 (ATG-021 untuk multiple myeloma), LILRB4 x CD3 (ATG-102 untuk leukemia myeloid akut dan leukemia myelomonositik kronis), dan FLT3 x CD3 (ATG-107 untuk leukemia myeloid akut).
, platform T cell engager 2.0 milik sendiri yang menampilkan pengikatan bivalen "2+1" untuk target yang mengekspresikan rendah, penyamaran hambatan sterik, dan urutan CD3 milik sendiri dengan kinetika on/off cepat untuk meminimalkan sindrom pelepasan sitokin (CRS) dan meningkatkan kemanjuran. Karakteristik ini mendukung penerapan platform yang luas di seluruh penyakit autoimun, tumor padat, dan keganasan hematologi, dengan program yang menargetkan CD19 x CD3 (ATG-201 untuk penyakit autoimun terkait sel B), CDH6 x CD3 (ATG-106 untuk kanker ovarium dan kanker ginjal), ALPPL2 x CD3 (ATG-112 untuk tumor ginekologi dan kanker paru-paru sel bukan kecil), LY6G6D x CD3 (ATG-110 untuk kanker kolorektal stabil mikrosatelit), GPRC5D x CD3 (ATG-021 untuk multiple myeloma), LILRB4 x CD3 (ATG-102 untuk leukemia myeloid akut dan leukemia myelomonositik kronis), dan FLT3 x CD3 (ATG-107 untuk leukemia myeloid akut).
Hingga saat ini, Antengene telah memperoleh 32 persetujuan obat baru investigasi (IND) di AS dan Asia, dan memperoleh persetujuan aplikasi obat baru (NDA) di 10 pasar Asia Pasifik. Aset komersial utamanya, XPOVIO® (selinexor), disetujui di Daratan Tiongkok, Taiwan Tiongkok, Hong Kong Tiongkok, Makau Tiongkok, Korea Selatan, Singapura, Malaysia, Thailand, Indonesia, dan Australia, dan telah dimasukkan dalam skema asuransi nasional di lima pasar tersebut (Daratan Tiongkok, Taiwan Tiongkok, Australia, Korea Selatan, dan Singapura).
Pernyataan berwawasan ke depan
Pernyataan berwawasan ke depan yang dibuat dalam artikel ini hanya berkaitan dengan peristiwa atau informasi pada tanggal pernyataan dibuat dalam artikel ini. Kecuali sebagaimana disyaratkan oleh hukum, kami tidak berkewajiban untuk memperbarui atau merevisi secara publik pernyataan berwawasan ke depan apa pun, baik sebagai hasil dari informasi baru, peristiwa masa depan, atau lainnya, setelah tanggal pernyataan dibuat atau untuk mencerminkan terjadinya peristiwa yang tidak diantisipasi. Anda harus membaca artikel ini secara lengkap dan dengan pemahaman bahwa hasil atau kinerja masa depan kami yang sebenarnya dapat berbeda secara material dari apa yang kami harapkan. Dalam artikel ini, pernyataan tentang, atau referensi kepada, niat kami atau niat Direktur kami atau Perusahaan kami dibuat pada tanggal artikel ini. Setiap niat ini dapat berubah mengingat perkembangan masa depan. Untuk pembahasan lebih lanjut tentang faktor-faktor ini dan faktor-faktor lain yang dapat menyebabkan hasil masa depan berbeda secara material dari pernyataan berwawasan ke depan apa pun, silakan lihat risiko dan ketidakpastian lain yang dijelaskan dalam Laporan Tahunan Perusahaan untuk tahun yang berakhir pada 31 Desember 2024, dan dokumen-dokumen yang kemudian diserahkan ke Bursa Efek Hong Kong.
Untuk informasi lebih lanjut, silakan hubungi:
Kontak Investor:
Donald Lung
E-mail: donald.lung@antengene.com
Kontak BD:
Ariel Guo
E-mail: ariel.guo@antengene.com
![]() Lihat konten asli untuk mengunduh multimedia:https://www.prnewswire.com/news-releases/xpovio-receives-reimbursement-approval-in-south-korea-for-a-second-multiple-myeloma-indication-302700200.html
Lihat konten asli untuk mengunduh multimedia:https://www.prnewswire.com/news-releases/xpovio-receives-reimbursement-approval-in-south-korea-for-a-second-multiple-myeloma-indication-302700200.html
SUMBER Antengene Corporation Limited
Anda Mungkin Juga Menyukai

Analis Berpengalaman Sebut Bitcoin Benar-Benar Terjebak di Area Ini
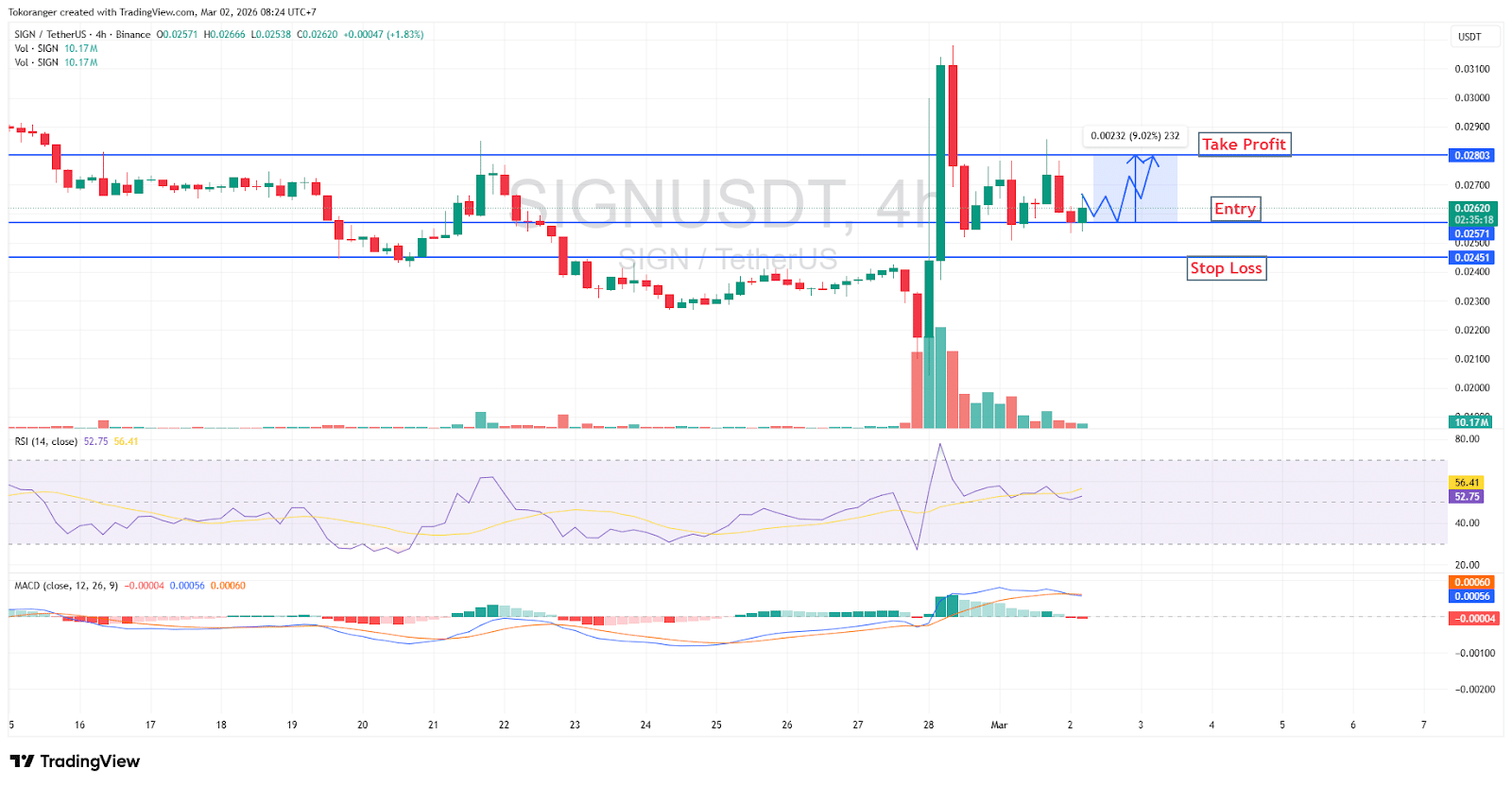
Sinyal Kripto 2 Maret 2026: Analisis Teknikal dan Proyeksi Pasar
